La revista Nature ha publicado esta semana un pionero modelo de desarrollo humano temprano nunca antes observado debido a las restricciones éticas en el uso de embriones en investigación. Dicho modelo, que utiliza células madre humanas, tiene un enorme potencial para entender las causas de los defectos de nacimiento y mejorar el estudio de enfermedades.
Al principio del desarrollo, cuando el embrión humano es apenas una pequeña bola de células, se dobla sobre sí mismo para formar una estructura de tres capas con un extremo delantero y otro trasero, llamada gastrula. Este proceso se llama gastrulación, y las capas pasan a formar los diferentes tipos de tejido del cuerpo: el ectodermo da lugar al sistema nervioso, el mesodermo a los músculos y el endodermo al intestino.
Aunque se habían hecho estándares en 3D de este proceso utilizando células de ratones, estos poseen limitaciones para estudiar el desarrollo humano. Científicos de la Universidad de Cambridge (Reino Unido), liderados por el español Alfonso Martínez Arias, han desarrollado un nuevo modelo del desarrollo embrionario temprano en nuestra especie.
“La gastrulación es el momento clave de la embriogénesis. Es cuando surge el organismo en sí, cuando se organizan las células con respecto a una serie de ejes virtuales que organizarán el desarrollo de tejidos y órganos”, explica a Sinc Martínez Arias.
El equipo ha logrado generar estructuras tridimensionales –llamadas gastruloides– a partir de células madre de embriones humanos. Dicho modelo, publicado esta semana en la revista Nature, representa algunos elementos clave de un embrión de unos 18 a 21 días y permite observar los procesos que subyacen a la formación del cuerpo humano nunca antes observados.
Para los investigadores, un gastruloide de 3 días imita ciertas características clave de un embrión humano de 20 días. Así, sugieren que este modelo representa un primer paso hacia la modelización del cuerpo humano en 3D. “El conocimiento de estos procedimientos tiene el potencial de revelar las causas de los defectos de nacimiento y las enfermedades humanas, así como de crear pruebas para su detección en las mujeres embarazadas”.
“Este nuevo sistema modelo permitirá investigar por primera vez en el laboratorio los procesos del desarrollo embrionario humano temprano”, añade Naomi Moris, primera autora y experta de la Universidad de Cambridge.

Alfonso Martínez Arias y Naomi Moris. / University of Cambridge
Hasta ahora, la gastrulación se conocía como el período ‘caja negra’ del desarrollo humano, ya que las restricciones legales impiden el cultivo de embriones humanos en el laboratorio más allá del día 14 después de la fecundación, cuando comienza este proceso. Este límite moral –que no técnico– se estableció para que cayera en la etapa en que el embrión ya no puede formar un gemelo.
En los últimos años se han desarrollado varias técnicas para producir modelos similares a los embriones a partir de células madre animales y humanas. Esto ha llevado a los investigadores a pedir directrices específicas para proporcionar una supervisión ética más clara de este campo en rápido desarrollo. De momento, la legislación al respecto varía enormemente en los diferentes países.
“Nuestro trabajo permite estudiar de forma ética esta importante fase del desarrollo en humanos”, afirma Martínez Arias. “Hemos encontrado una manera de recapitular los elementos fundamentales de la gastrulación en nuestra especia, abriendo la posibilidad de analizar el momento en el que tienen su origen muchas patologías”.
Así, muchos defectos de nacimiento se originan durante este corto período, con causas que van desde la ingesta o exposición al alcohol, medicamentos, productos químicos e infecciones. Por eso, los autores subrayan que entender la gastrulación humana también podría arrojar luz sobre la infertilidad, el aborto espontáneo y los trastornos genéticos.
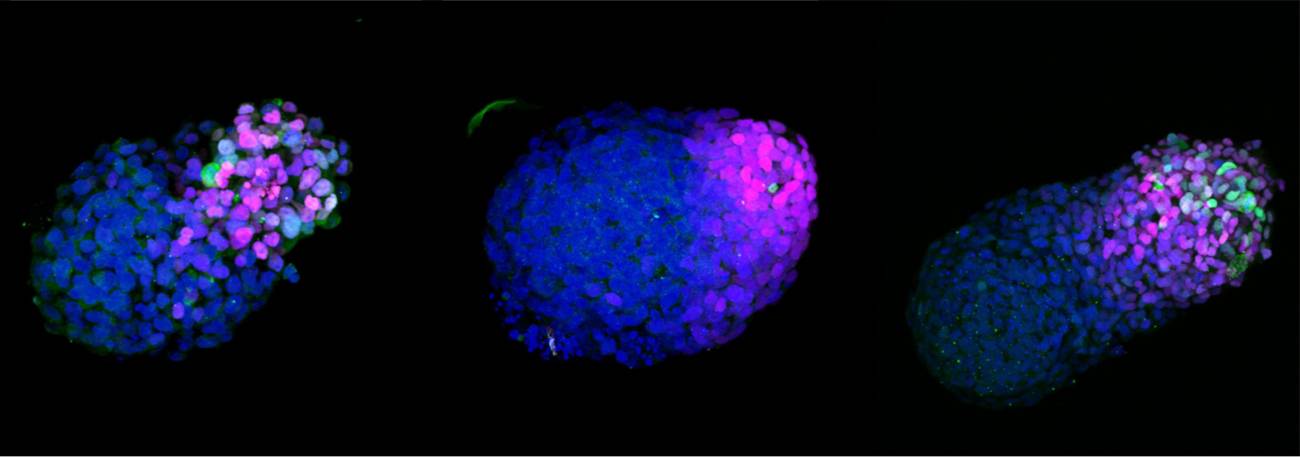
Gastruloide humano en crecimiento. 24h (izquierda), 48h (centro) y 72h (derecha) después de la agregación de células madre embrionarias (ESC). El azul marca el ADN, el magenta las células neurales (SOX2) y el verde las células mesodérmicas (BRA). / Naomi Moris
Los organismos modelo, incluyendo ratones y peces cebra, han permitido previamente a los científicos obtener algunos conocimientos sobre la gastrulación humana. Sin embargo, estos modelos pueden comportarse de manera diferente a los embriones humanos cuando las células comienzan a diferenciarse.
Un ejemplo es la talidomida, utilizada para el tratamiento de las náuseas en embarazadas. El fármaco pasó los ensayos clínicos tras ser probado en ratones, pero posteriormente provocó graves defectos de nacimiento en bebés. “Por esta razón es importante desarrollar mejores modelos de desarrollo humano”, subrayan los autores.
Los gastruloides no tienen el potencial de desarrollarse en un embrión completamente formado. No tienen células cerebrales ni ninguno de los tejidos necesarios para implantarse en el útero. Esto significa que nunca podrían pasar de las primeras etapas de desarrollo y, por lo tanto, se ajustan a las normas éticas actuales.
Referencia:
Moris, N. et al., ‘An in vitro model for anteroposterior organisation during human development.’ Nature, June 2020. DOI: 10.1038/s41586-020-2383-9