Investigadores de la Universidad Autónoma de Madrid han desarrollado una metodología que permite la activación de compuestos orgánicos con sílice para la obtención de moléculas orgánicas halogenadas, difíciles de obtener mediante otras metodologías. Los halógenos son elementos del grupo 17 de la tabla periódica, como el flúor y yodo.
La preparación de compuestos halogenados (con elementos del grupo 17 de la tabla periódica) es uno de los grandes retos de la química orgánica, ya que puede servir como punto de partida para la síntesis de moléculas mucho más complejas debido a su gran versatilidad bajo una gran cantidad de condiciones de reacción.
La instalación de halógenos de manera estereoselectiva (formación preferente de un estereoisómero sobre todos los posibles) ha atraído la atención de los químicos sintéticos durante los últimos años. Sin embargo, aunque la halogenación electrófila (en la que se utiliza la fuente de halógeno como electrófilo) ha sido ampliamente estudiada, la halogenación nucleófila (en la que se utiliza la fuente de halógeno como nucleófilo) no ha sido tan desarrollada.
El grupo de investigación FRONCAT del departamento de Química Orgánica de la Universidad Autónoma de Madrid (UAM), en un trabajo que publica la revista Chemical Communications, ahora ha llevado a cabo la halogenación nucleófila conjugada a distintos compuestos orgánicos.
El desarrollo de esta nueva metodología podría permitir la síntesis enantioselectiva, en un futuro, de compuestos orgánicos difíciles de obtener mediante metodologías clásicas. Los enantiómeros o isómeros ópticos son una clase de estereoisómeros tales que en la pareja de compuestos la molécula de uno es imagen especular de la molécula del otro y no son superponibles.
El método también podría ser aplicado en el proceso sintético de productos naturales o fármacos que requieran de la instalación estereoselectiva de un átomo de cloro o bromo con el fin de potenciar o modificar su actividad biológica.
Auxiliares quirales
En su trabajo, los investigadores se ayudaron de la presencia de un sulfóxido en el medio de reacción que actúa como promotor de la misma, permitiendo la liberación del halogenuro correspondiente a partir de un compuesto organosililado (compuesto orgánico con la presencia de uno o más átomos de silicio en su estructura), siendo este hecho la clave para la reacción.
“De esta manera logramos desarrollar un método general de halogenación nucleófila a distintos aceptores de Michael, que son moléculas orgánicas con la presencia de un doble enlace conjugado a un grupo atractor de electrones, como cetonas, ésteres o amidas, entre otros”, describen los autores.
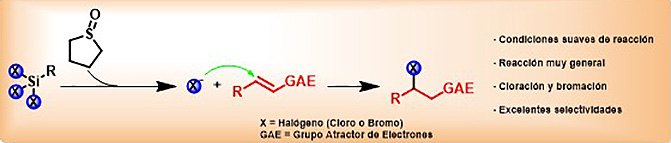
Resumen de la metodología desarrollada en el estudio. / UAM
Los investigadores consiguieron aplicar la metodología a la síntesis estereoselectiva de compuestos halogenados, para lo que se han utilizado compuestos orgánicos que presentan en su estructura un auxiliar quiral (compuesto químico o unidad que se incorpora temporalmente a una síntesis orgánica para que pueda llevarse a cabo de manera asimétrica). “Esto permite que, una vez la adición del halógeno se ha producido de manera selectiva por una de las dos caras de la molécula orgánica, se pueda obtener uno sólo de los dos enantiómeros posibles al eliminar el auxiliar quiral”.
La obtención estereoselectiva de moléculas orgánicas es de vital importancia para el desarrollo de nuevos fármacos. Esto es debido a que puede darse el caso en el que uno de los dos enantiómeros de la molécula tenga un efecto beneficioso para la salud mientras que el otro enantiómero tenga un ejemplo perjudicial.
Un ejemplo muy claro de este hecho es el fármaco conocido como Talidomida. En este caso, el fármaco se administraba en su forma racémica (es decir, los dos enantiómeros en proporción 50:50) como sedante para mujeres embarazadas. Sin embargo, posteriormente se descubrió que uno de los dos enantiómeros producía el efecto buscado, mientras que el otro producía malformaciones en los fetos.
La metodología desarrollada para la obtención estereoselectiva de compuestos halogenados mediante el uso de auxiliares quirales presenta una gran importancia, ya que de manera ideal sólo se obtendría uno de los dos enantiómeros.
Adicionalmente, en el trabajo se ha llevado a cabo la derivatización de estos últimos compuestos para la obtención de ácidos carboxílicos halogenados y halo alcoholes enantioméricamente enriquecidos, los cuales se tratan de compuestos de gran interés dentro del campo de la química orgánica.
Referencia bibliográfica:
Víctor Laina-Martín, Ignacio Pérez, José A. Fernández-Salas and José Alemán. "Nucleophilic halo-Michael addition under Lewis-base activation". Chem. Commun., 2019, 55, 12936-12939.