Los peces óseos u osteictios, como el pequeño pez cebra (o danio cebrado), muestran una habilidad que para los mamíferos no es más que un sueño: si seccionamos un trozo de su corazón, nadarán con dificultad durante unos días, pero un mes después su estado será totalmente normal. Una de las preguntas que se plantea hoy la medicina regenerativa es por qué los humanos no pueden hacerlo.
Las células del músculo cardíaco ayudan a regenerar los corazones dañados del pez cebra. Así concluyen dos estudios, publicados esta semana en la revista Nature, que proporcionan nuevas pistas sobre cómo imitar a estos animales y conseguir que los corazones humanos heridos puedan regenerarse.
El pez cebra puede regenerar de manera eficiente el músculo cardíaco perdido, pero hasta el momento no estaba claro el tipo de célula responsable de la sustitución de estos cardiomiocitos. Ambos trabajos sugieren que, al menos en el pez cebra, la regeneración cardíaca no implica necesariamente la activación de una población de células madre.
El primero de los trabajos, dirigido por Kenneth D. Poss, investigador de la Universidad de Duke (EE UU), demuestra que la mayor parte de la regeneración es llevada a cabo por un tipo particular de cardiomiocitos. Las células, que expresan el gen cardiogénesis gata4, entran en la zona dañada donde proliferan y ayudan a reconstruir el músculo cardíaco.
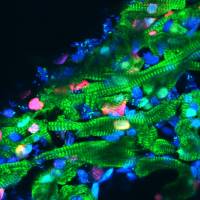
Imagen confocal de cardiomicitos identificados de pez cebra.
Por su parte, Juan Carlos Izpisúa Belmonte, investigador del Instituto Salk de Estudios Biológicos en California (EE UU) y el Centro de Medicina Regenerativa de Barcelona (CMRB) y líder del segundo estudio publicado en Nature, está de acuerdo en que estas células se desdiferencian y proliferan con el fin de reparar y regenerar el músculo cardíaco.
Aunque se muestra optimista respecto a los resultados, el científico español también cree que los investigadores deberían tomarse estos resultados como una advertencia para no pasar por alto la contribución a la regeneración que podrían hacer las células maduras.
“La regeneracion del corazon en el pez no ocurre mediante el uso de células madre o células progenitoras, sino por la dediferenciación de cardiomiocitos preexistentes en el corazón”, explica Izpisúa. "Nuestros resultados sugieren que quizás la regeneración en mamíferos no es una utopía y que un conocimiento más profundo de los mecanismos moleculares que inducen la proliferación de los cardiomiocitos podría ayudarnos a entender la falta de regeneración en humanos, y eventualmente, a tratar de modificar ese proceso".
Cardiomiocitos transgénicos
Para determinar qué células repararon en realidad el músculo cardíaco extirpado de los peces cebra, el equipo de Izpisúa Belmonte utilizó técnicas de ingeniería genética para convertir a los cardiomiocitos en "transgénicos", insertándoles un gen trazador o identificador, que les otorgaba una fosforescencia verdosa al microscopio.
Después, cortaron un 20% de cada ventrículo de los peces y esperaron un par de semanas a que los corazones se regenerasen: si el músculo cardíaco no brillaba, significaría que las células responsables de la reparación del tejido muscular dañado no eran los cardiomiocitos sino otras, como las células madre cardíacas.
Pero se toparon con un sorprendente descubrimiento. Los cardiomiocitos ya desarrollados que quedaban tras la herida retornaron a un estado más joven, comenzaron a dividirse para reemplazar las células perdidas y volvieron a madurar por segunda vez, convirtiéndose en tejido muscular cardíaco nuevo.
Los corazones humanos no pueden emprender por sí solos estas transformaciones regenerativas. Cuando resulta dañado por un ataque al corazón, el tejido muscular cardíaco se sustituye por tejido cicatricial, incapaz de contraerse. Sin embargo, antes de llegar a la insuficiencia cardíaca, las células musculares cardíacas dañadas de los mamíferos entran en un estado de autopreservación conocido como "hibernación", en el que dejan de contraerse y se esfuerzan por sobrevivir.
"Nuestra hipótesis es que los cardiomiocitos en hibernación de los mamíferos podrían ser células que están intentando reproducirse", añade Chris Jopling, autora principal del estudio y estudiante de postdoctorado con Izpisúa Belmonte en el CMRB, que considera que la "hibernación" del corazón humano es significativa. "Tal vez lo único que necesiten sea un pequeño empujón en la buena dirección".
---------
Referencias bibliográficas:
Kenneth D. Poss et al.: “Primary contribution to zebrafish heart regeneration by gata41 cardiomyocytes”. Nature, 25 de marzo de 2010.
Juan Carlos Izpisúa Belmonte et al.: “Zebrafish heart regeneration occurs by cardiomyocyte dedifferentiation and proliferation”. Nature, 25 de marzo de 2010.