Investigadores de un consorcio internacional han utilizado dos anticuerpos neutralizantes de pacientes recuperados y los han combinado con sus regiones de unión al virus, con el objetivo de eliminar la infección en ratones enfermos y proteger a los no infectados. Ahora trabajan para desarrollar una versión más estable que pueda probarse en ensayos clínicos con humanos.
Un equipo del consorcio Prometheus ha revelado cómo los anticuerpos neutralizan el virus de la fiebre hemorrágica de Crimea-Congo (FHCC), un virus zoonótico muy extendido y transmitido por garrapatas.
Los mecanismos descubiertos por los investigadores para la neutralización de este virus altamente patógeno proporcionan una base para la preparación ante epidemias, según los autores. Los resultados se han publicado en el último número de la revista Science.
Este virus es endémico en África, Asia y Europa. Los investigadores indican que el calentamiento global está facilitando la propagación del vector de la garrapata en nuevos hábitats transportado por aves migratorias, como mostró el brote del pasado junio en España. En ese mes se detectaron dos contagios, de un ganadero en Salamanca y una senderista en el Bierzo. Los dos sobrevivieron.
La infección en humanos puede causar una enfermedad grave que acaba provocando la muerte en cerca del 30 % de los casos diagnosticados. La OMS ha incluido al virus FHCC como patógeno prioritario en su plan de investigación y desarrollo.
En este estudio, los científicos han utilizado lo que denominan virología estructural para reconstruir los primeros mapas a escala atómica en 3D, o estructuras, de una parte del virus causante de la infección que le permite infectar las células del huésped.
El equipo también determinó cómo dos anticuerpos neutralizantes, extraídos de pacientes recuperados, interrumpen la capacidad del virus para infectar una célula, lo que, junto con la información estructural, ofrece ideas para desarrollar terapias contra el virus.
La investigación se hace eco de un enfoque clave que los autores, entre ellos el biólogo molecular Jason McLellan —especializado en la estructura y la función de las proteínas víricas, incluidas las de los coronavirus— han utilizado para luchar contra la covid-19 y el virus respiratorio sincitial.
“La fiebre hemorrágica de Crimea-Congo es una enfermedad terrible. Con la virología estructural, estamos descubriendo los secretos de estas proteínas en la superficie de los virus y sus vulnerabilidades, y eso nos ayuda a construir mejores terapias con anticuerpos y vacunas”, subraya McLellan.
Dirigido por Kartik Chandran, microbiólogo e inmunólogo de la Facultad de Medicina Albert Einstein, el equipo Prometheus está formado por el laboratorio de McLellan y otros laboratorios académicos, empresas de biotecnología y el Instituto de Investigación Médica de Enfermedades Infecciosas del Ejército de Estados Unidos.
El consorcio identificó previamente dos anticuerpos de pacientes recuperados de la FHCC que neutralizaron el virus de forma potente. A continuación, combinaron las regiones de unión al virus de los dos anticuerpos para producir un “anticuerpo biespecífico” que elimina las infecciones en ratones enfermos y protege a los ratones no infectados del virus FHCC. Ahora están trabajando para desarrollar una versión más estable que pueda probarse en ensayos clínicos con humanos.
“Supongamos que un investigador, un trabajador sanitario o un militar de Estados Unidos tiene que visitar Oriente Medio o África”, explica Akaash Mishra, estudiante de postgrado de la Universidad de Texas en Austin en el laboratorio de McLellan y primer autor del trabajo. "Antes de ir, podrían recibir una inyección profiláctica con uno de estos anticuerpos para protegerse de la infección. Esto se llama inmunización pasiva y les protegería durante varias semanas o meses".
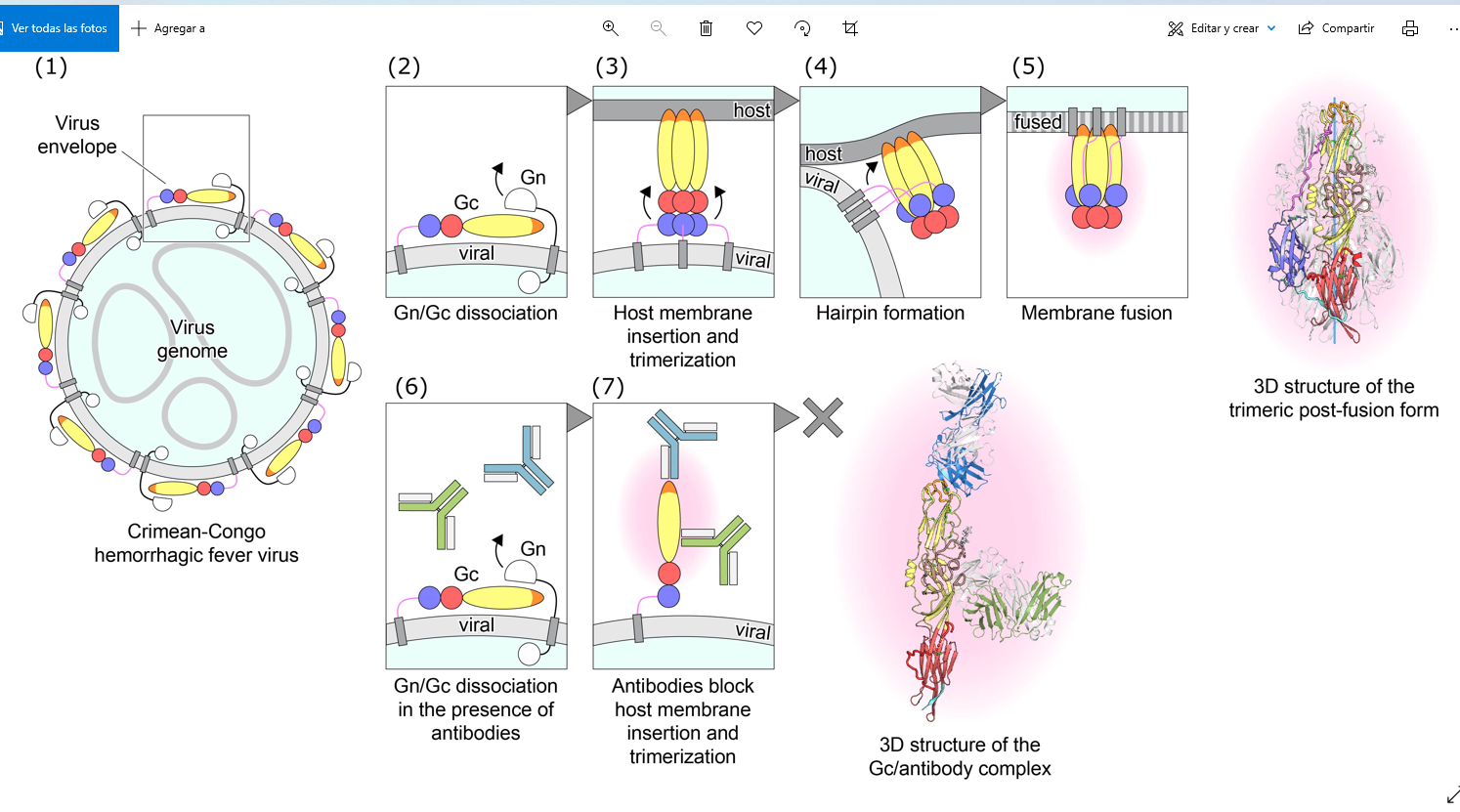
Neutralización sinérgica del virus de la fiebre hemorrágica de Crimea-Congo por dos anticuerpos monoclonales. / Akaash K. Mishra & Jan Heller
El anticuerpo biespecífico también podría ayudar a los pacientes ya infectados por la FHCC a recuperarse de la infección y prevenir la mortalidad. Los resultados de la investigación también podrían utilizarse para la creación de una futura vacuna, afirman los autores.
El virus de la fiebre hemorrágica de Crimea-Congo depende de una molécula que cambia de forma en su superficie, llamada proteína Gc, para fusionarse con las células huésped. A fin de impedir que el virus infecte una célula, un agente terapéutico debe dirigirse a la forma de prefusión de la proteína.
El laboratorio de McLellan utilizó la cristalografía de rayos X para determinar la estructura de la proteína Gc de prefusión unida a anticuerpos neutralizantes de pacientes recuperados. Por su parte, el laboratorio de Félix Rey, virólogo estructural del Instituto Pasteur, determinó la forma posterior a la fusión.
Mediante el estudio de las formas de prefusión y postfusión y la localización de los puntos de unión de varios anticuerpos, los investigadores determinaron que un anticuerpo impide que la proteína Gc cambie a la forma postfusión, y el otro impide que inserte parte de sí misma en la membrana de una célula huésped. Esto ayuda a explicar por qué estos dos anticuerpos combinados son tan eficaces para impedir que el virus infecte las células.
La FHCC se transmite principalmente a través de las garrapatas, y los expertos en enfermedades infecciosas advierten que la amenaza del virus podría crecer, ya que la garrapata responsable de su propagación se encuentra en más lugares, debido al cambio climático y otros factores.
“No mucha gente había oído hablar de los coronavirus antes de que la covid-19 se convirtiera en una pandemia”, advierte Mishra. “Creo que debemos estar mejor preparados con este tipo de virus emergentes, que tal vez no estén causando una epidemia en este momento, pero que aún tienen un gran potencial para futuros brotes”.